Centrum Medycyny Doświadczalnej IMDiK PAN

Centrum Medycyny Doświadczalnej CePT (CMD-CePT) to zespół laboratoriów środowiskowych powstałych w Instytucie Medycyny Doświadczalnej i Klinicznej im. M. Mossakowskiego PAN w ramach projektu Centrum Badań Przedklinicznych i Technologii (CePT).
W ramach Centrum Medycyny doświadczalnej funkcjonują następujące laboratoria:
Środowiskowe Laboratorium Badań Toksykologicznych (LBT)
Rynek usług toksykologicznych w Polsce, w Europie i na świecie jest bardzo rozwinięty. O ile wykonywanie prostych badań toksykologicznych (typu wyznaczania LD50) jest oferowane zarówno w Europie, jak i w Polsce – to badanie potencjału pro- bądź antykarcinogennego na modelach transgenicznych jest usługą bardzo deficytową.
Laboratorium Badań Toksykologicznych wykonuje analizy bezpieczeństwa przedklinicznego nowych leków i substancji chemicznych w zakresie wymagań objętych panelem toksykologii regulacyjnej – zgodnie z zasadami Dobrej Praktyki Laboratoryjnej (GLP). Ze względu na zaplecze w postaci zwierzętarni w której prowadzone są hodowle genetycznie zmodyfikowanych gryzoni laboratorium specjalizuje się w ocenach toksyczności substancji przy użyciu zwierząt transgenicznych.
Profil badawczy:
- Przeprowadzenie testów cytotoksyczności w warunkach in vitro na hodowlach komórkowych ludzkich lub zwierzęcych.
- Ocenę histopatologiczna materiału pobranego od zwierząt.
Laboratorium oferuje:
- hodowlę linii komórkowych
- przeprowadzenie testów oceniających wpływ związków na proliferację komórek (test MTT, XTT, Ki67 i inne)
- obrazowanie komórek w określonym zakresie fali (dostępne filtry fluorescencji: DAPI, GFP, TexasRed) i ocena statystyczna materiału z wykorzystaniem aparatu Cytation-3
- genotypowanie
- bankowanie materiału biologicznego
- wykonanie preparatu histopatologicznego (cięcie na kriostacie zakres cięcia1-100µm, podstawowe barwienia) i ocena mikroskopowa z zapisem cyfrowym zdjęć
Realizowane projekty badawcze we współpracy z Środowiskowym Laboratorium Hodowli Zwierząt Genetycznie Modyfikowanych:
- Badania przedkliniczne i kliniczne kandydata na innowacyjny lek w terapii astmy i nieswoistych chorób zapalnych jelit (nr projektu: POIR.01.01.01-00-0168/15)
- Opracowanie kandydata na lek „first-in-class” w terapii idiopatycznego włóknienia płuc w oparciu o substancje czynne blokujące chitotriozydazę (POIR.01.01.01-00-0551/15)
Środowiskowe Laboratorium Rezonansu Magnetycznego Małych Zwierząt (LRM)
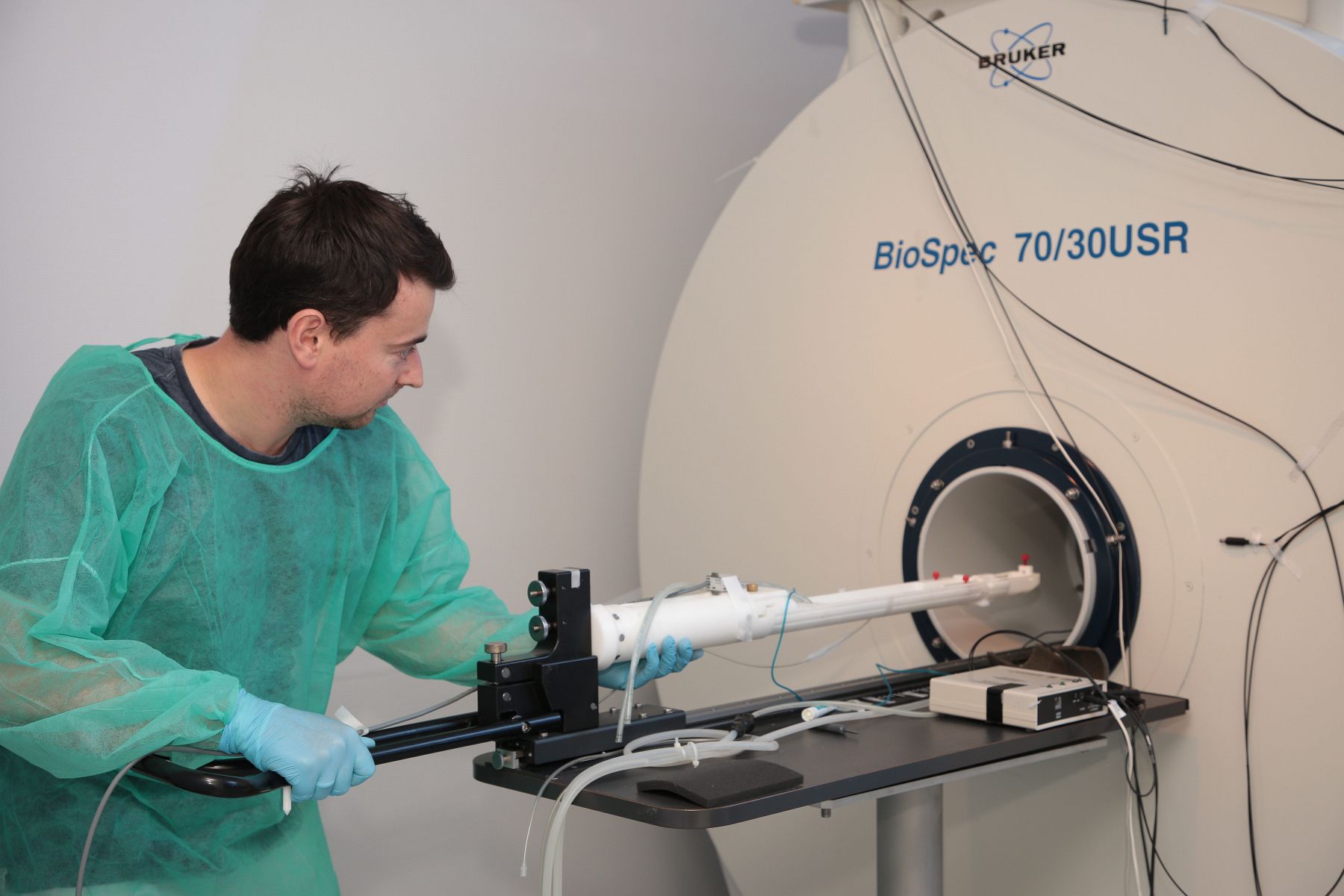
Laboratorium jest wyposażone w tomograf rezonansu magnetycznego firmy Bruker, model Biospec 70/30USR o indukcji pola magnetycznego 7T. Aparat ten jest przeznaczony do badania zwierząt laboratoryjnych (przede wszystkim myszy i szczurów), ale umożliwia też badanie tkanek ex vivo czy próbek materiałów. LRM to obecnie jedna z dwóch jednostek w Polsce wyposażona w sprzęt tej klasy.
Główne cechy tomografu rezonansowego Bruker Biospec to:
 wartość indukcji pola głównego: 7T
wartość indukcji pola głównego: 7T- maksymalny gradient pola cewek gradientowych: 300mT/m
- pasmo toru nadawczo-odbiorczego: 5-300,3 MHz (pozwala na detekcję: 1H, 3He, 13C, 15P, 129Xe)
- średnica otworu: 310 mm
- maksymalna średnica do wykorzystania w czasie obrazowania: 154 mm
Posiadany sprzęt pozwala na wykonywanie obrazowania T1 i T2, obrazowania dynamicznego z podaniem środka cieniującego, obrazowania ze wzmocnieniem kontrastowym, spektroskopii zlokalizowanej , obrazowania dyfuzyjnego, angiografii i wielu innych badań.
Laboratorium posiada bogato wyposażone zaplecze do obsługi doświadczeń. Najważniejszy sprzęt to:
- mikroskop operacyjny z kamerą
- sterowany komputerowo aparat stereotaktyczny
- dwa aparaty do anestezji wziewnej (izofluranowej)
- pulsoksymetr do monitorowania zwierząt w trakcie zabiegów
Jako jedyne w Polsce, Laboratorium jest przygotowane do wykonywania badań w wysokim standardzie higienicznym, również do wykonywania badań zwierząt o obniżonej odporności. Pomieszczenie do aklimatyzacji zwierząt za barierą sanitarną jest wyposażone w regały do obsługi klatek indywidualnie wentylowanych (individually ventilated cages, IVC) oraz stację do wymiany klatek z przepływem laminarnym powietrza. Możliwe jest też wykonywanie zabiegów chirurgicznych w warunkach aseptycznych.
Przykładowe projekty:
- Korelaty zmian magnetyczno-rezonansowych w mózgach zwierząt na diecie wysokotłuszczowej: obraz histologiczny i zachowanie (Narodowe Centrum Nauki, grant 2011/03/B/NZ4/03771) – kier. dr Stefan Gaździński (Wojskowy Instytut Medycyny Lotniczej).
- Biowskaźniki procesów neurodegeneracji i endogennej neuroprotekcji w padaczce (Narodowe Centrum Nauki, grant 2011/01/M/NZ4/04916) – kier. prof. Konrad Rejdak (IMDiK PAN, Uniwersytet Medyczny w Lublinie).
- Kontrolowanie głębokości lokalnej nekrozy indukowanej w wątrobie szczura in vivo nieliniową ogniskowaną wiązką ultradźwiękową z elektronicznie sterowanym ogniskiem (Narodowe Centrum Nauki, grant 2011/01/B/ST7/06735) – kier. dr Tamara Kujawska (Instytut Podstawowych Problemów Techniki PAN).
- Przebieg pozasiatkówkowej neurodegeneracji w modelu spontanicznej jaskry (myszy DBA/2J) – przyżyciowe badania metodami rezonansu magnetycznego (Narodowe Centrum Nauki, grant 2012/07/D/NZ4/04199) – kier. dr Michał Fiedorowicz (IMDiK PAN).
- Antyhipertensyjna skuteczność peptydów z nasion rzepaku u szczurów. Potencjalna rola nowych mechanizmów konwersji ang I. (Narodowe Centrum Nauki, grant 2011/01/B/NZ4/05703) – kier. prof. Elżbieta Kompanowska-Jezierska (IMDiK PAN)
- Rola mózgowej asymetrycznej dwumetyloargininy (ADMA) w encefalopatii wątrobowej: marker, mediator czy regulator? (Narodowe Centrum Nauki) – kier. dr hab. Magdalena Zielińska.
- MRI navigated enhancement of mesenchymal stem cell (MSC) homing towards stroke lesion – evaluating an impact on animal recovery with behavioral testing and imaging (Narodowe Centrum Badań i Rozwoju) – kier. prof. Barbara Łukomska (IMDiK PAN).
- Wpływ obniżonej projekcji noradrenergicznej na pamięć w mysim modelu choroby Parkinsona – badania behawioralne i neuroobrazowe (Warszawski Uniwersytet Medyczny, projekt 1M9/PM11/14) – kier. dr Małgorzata Zaremba (IMDiK PAN, Warszawski Uniwersytet Medyczny).
Środowiskowe Laboratorium Syntez Chemicznych (LSC)
Laboratorium jest przeznaczone do otrzymywania w standardzie GMP (Good Manufacturing Practice) substancji do badań przedklinicznych i klinicznych oraz leków z grupy tzw. sierocych. Laboratorium specjalizuje się w syntezie/oczyszczaniu biologicznie czynnych peptydów, peptydomimetyków i innych związków heterocyklicznych. Usługi polegające na kontraktowej syntezie eksperymentalnych substancji biologicznie czynnych w standardzie GMP są dość trudno dostępne w skali światowej, a w Polsce jest to jednostka unikalna.
Laboratorium przeznaczone jest do prowadzenia prac badawczo – rozwojowych i produkcyjnych zgodnie ze standardem Dobrej Praktyki Laboratoryjnej (Good Laboratory Practice) w zakresie substancji czynnych przeznaczonych do badań przedklinicznych (np. badania toksykologiczne) i klinicznych.
Laboratorium wyposażone jest w nowoczesną aparaturę umożliwiającą otrzymywanie i oczyszczanie związków w skali półtechnicznej tj. reaktory, homogenizator, chromatografy i wirówki, a także własne zaplecze analityczne (m.in. HPLC-MS).
Laboratorium jako odpowiedź na potrzeby rynku.
Nowe substancje czynne będące wynikiem prac R&D jednostek naukowych i badawczych, przed ich komercjalizacją, wymagają przeprowadzenia badań przedklinicznych oraz klinicznych. W tym celu konieczne jest wyprodukowanie substancji API w ilościach przekraczających możliwości typowych laboratoriów naukowych. W obecnej chwili potencjalni nabywcy wynalazków na etapie badań laboratoryjnych wymagają prowadzenia procesów zgodnie ze standardami GMP lub GLP zapewniającymi wysoką jakość i wiarygodność prowadzonych badań. Laboratorium odpowiada na te potrzeby poprzez udostępnianie zaplecza aparaturowo-kadrowego dostosowanego do podwyższonych rygorów badawczych zapewniających powtarzalne i wiarygodne wyniki badań.
Oferta Laboratorium obejmuje:
- Prowadzenie procesu syntezy i oczyszczania produktów w oparciu o standardy GLP.
- Dostosowanie przepisów technologicznych do standardów GLP.
- Skalowanie procesów.
Środowiskowe Laboratorium Hodowli Zwierząt Genetycznie Modyfikowanych (LHZ)
Hodowla zwierząt doświadczalnych genetycznie modyfikowanych (transgeniczne, knock-out, knock-in, bezgrasicze, itp.).
Prognozy dotyczące wykorzystywania zwierząt w badaniach biomedycznych wskazują, że udział zwierząt modyfikowanych genetycznie będzie w nadchodzących latach dynamicznie wzrastał (np. w Wielkiej Brytanii już w tej chwili wynosi 40%).
Unowocześnienie sposobu działania zwierzętarni (wprowadzenie klatek i regałów indywidualnie wentylowanych IVC) umożliwi rozwój hodowli zwierząt specjalnych dla potrzeb naszego instytutu, innych ośrodków z Kampusu Ochota, oraz innych odbiorców. Docelowo laboratorium uzyska dla swoich działań hodowlanych certyfikat GLP (Good Laboratory Practice).
